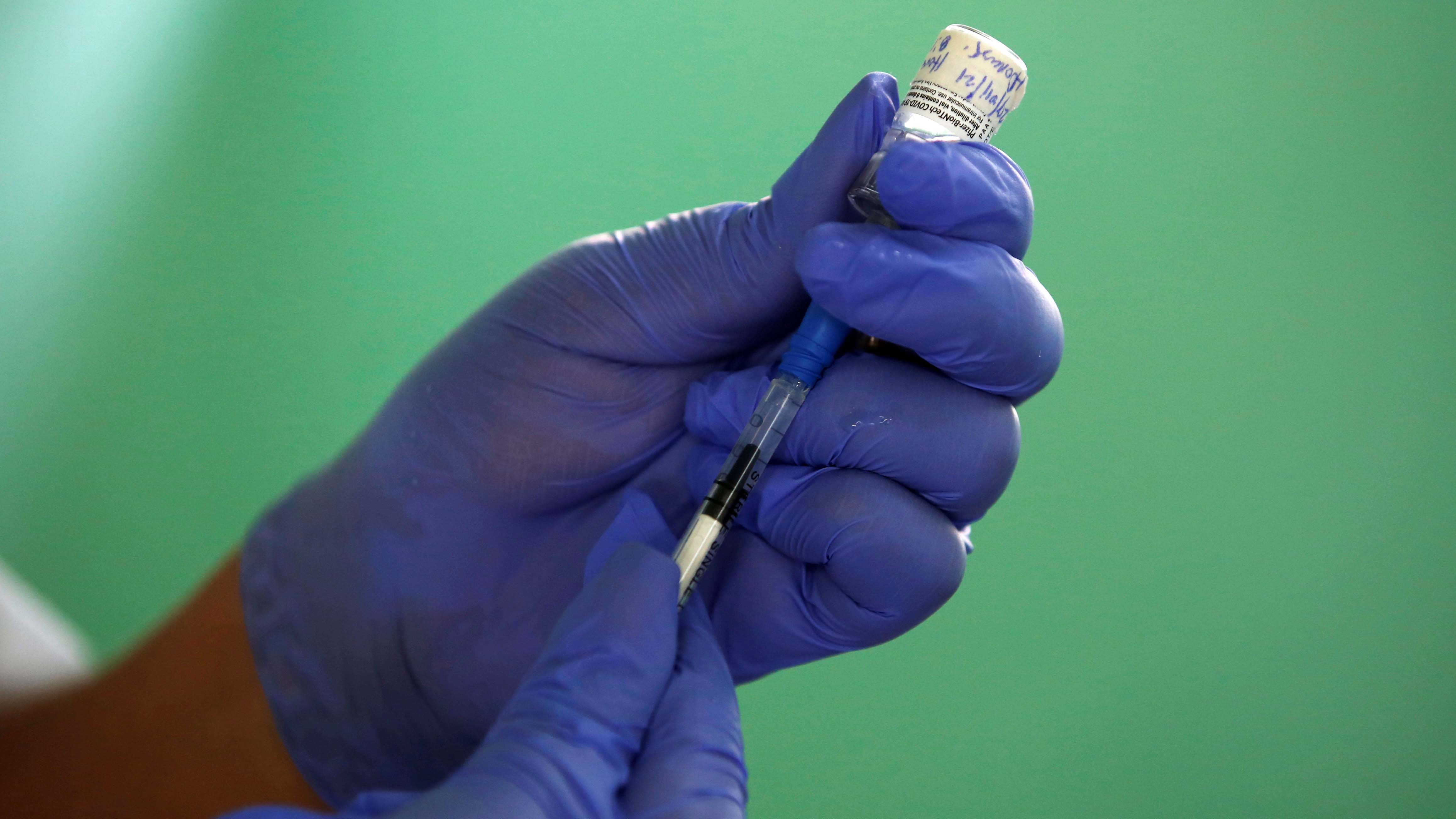
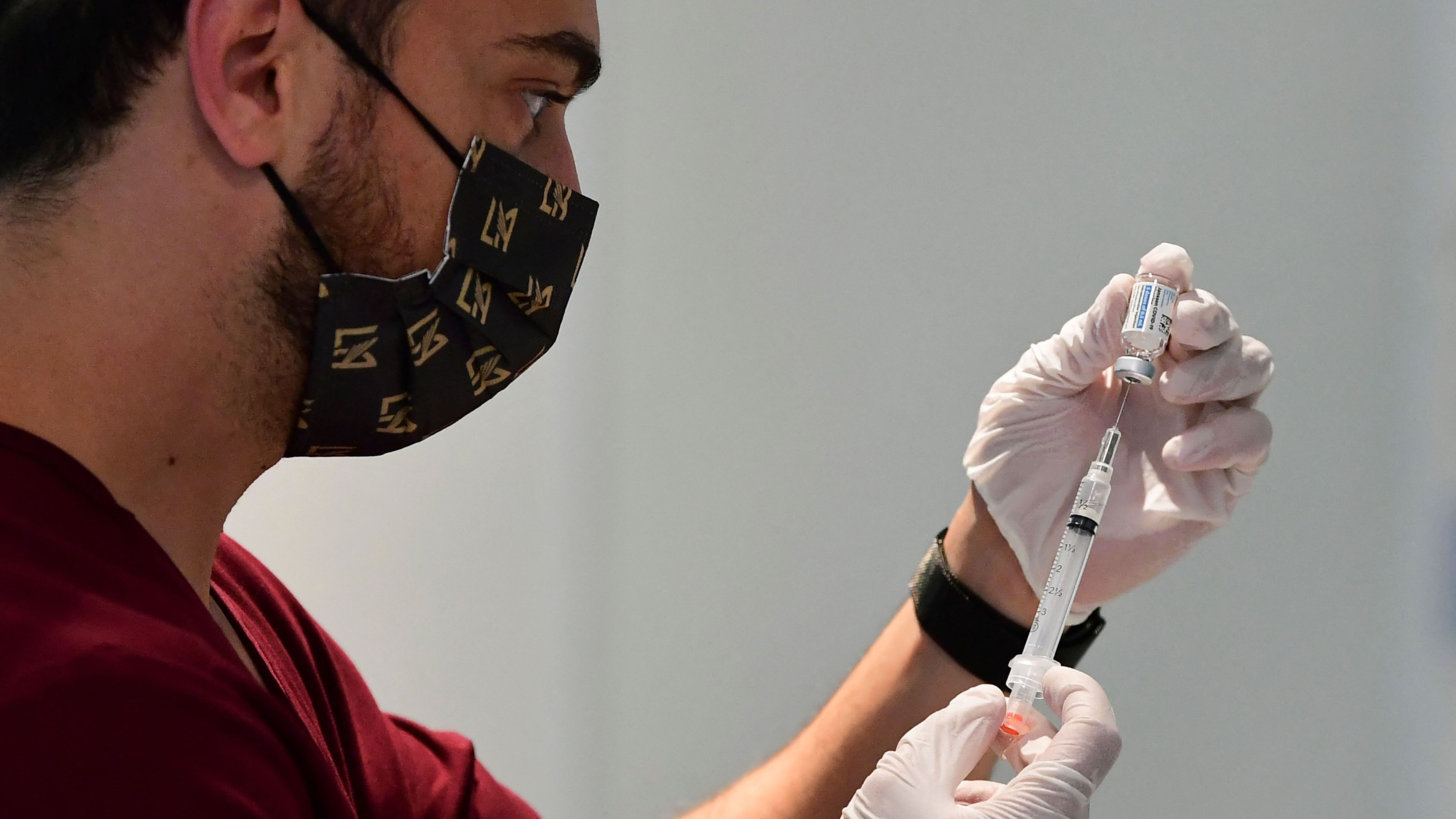
La Administración de Alimentos y Medicamentos (FDA, por sus siglas en inglés) concedió este lunes autorización para uso de emergencia de la vacuna contra el COVID-19 de Pfizer para menores de entre 12 y 15 años.
De esta forma la FDA actualizó el permiso que dio a Pfizer en diciembre pasado, cuando solo la autorizó para mayores de 16 años.
"La ampliación de la autorización para uso de emergencia de la vacuna contra el COVID-19 de Pfizer-BioNTech es una medida significativa en la lucha contra la pandemia", afirmó la comisionada en funciones de la FDA, Janet Woodcock, en un comunicado.
La comisionada aseguró también que "padres y tutores pueden estar seguros de que la agencia llevó a cabo una revisión rigurosa y exhaustiva de todos los datos disponibles" antes de tomar la decisión de autorizar la vacuna para ese grupo de menores.
Canadá se convirtió la semana pasada en el primer país del mundo en autorizar el preparado de Pfizer para mayores de 12 años, después de que la farmacéutica anunciara a finales de marzo una eficacia del 100 % en un estudio a 2,260 individuos en ese grupo de edad.
Pfizer era la única vacuna de las tres autorizadas por la FDA en Estados Unidos (las otras dos son la de Moderna y la de Johnson & Johnson) que estaba disponible para adolescentes de 16 y 17 años.
Según datos de los Centros para el Control y la Prevención de Enfermedades (CDC, por sus siglas en inglés), más de 2.4 millones de estos jóvenes en el país habían recibido hasta este lunes al menos una dosis del preparado de Pfizer.
Pfizer también inició ensayos clínicos de su vacuna en niños de entre 6 meses y 11 años.
Según los expertos, la inmunización de niños, que suponen alrededor de un 20% de la población de Estados Unidos, es esencial para poner fin a la pandemia de coronavirus, y señalan que es poco probable que el país alcance la inmunidad colectiva hasta que los menores sean también vacunados.